Tartalom
A BRAF-teszteket a daganatok genetikai változásainak (genomiális változások) keresésére végzik, amelyek egyes rákos megbetegedésekben jelen vannak, beleértve az áttétes melanomát, a tüdőrákot, a vastagbélrákot és másakat. Ha pozitív, a BRAF mutáció jelenléte segíthet a kezelés irányításában (például a BRAF mutációkat célzó gyógyszerek), a prognózis becslésében és egyebekben. A teszt elvégezhető különböző technikákkal, például immunhisztokémiával vagy átfogó genetikai profilalkotással, és elvégezhető tumormintán vagy vérvizsgálattal (folyékony biopszia).
A teszt célja
BRAF-tesztet végeznek a tumor BRAF-mutációinak keresésére. A BRAF onkogén egy olyan fehérjét kódol, amely fontos néhány rák növekedésében. Ezeket a mutációkat általában egy sejt rákossá válásának folyamatában szerzik be. A rák hátterében ezek a mutációk általában nem örökletesek.
Néhány ok, amiért a BRAF teszt elvégezhető, a következők:
- A kezelés irányításához a BRAF megcélzására tervezett gyógyszerekkel (BRAF és MEK inhibitorok). Ez igaz számos metasztatikus daganatra, de a 3. stádiumú melanómára is, amely a melanoma adjuváns terápiáját irányítja.
- Megjósolni a választ a nem célzott terápiás kezelésekhez. A BRAF mutáció jelenléte megjósolhatja, hogy egy személy reagál-e bizonyos típusú kemoterápiára stb.
- A prognózis becsléséhez. A BRAF-mutációkat tartalmazó daganatok történelmileg rosszabb prognózissal rendelkeztek, mint a mutáció nélküliak, bár ez a mutációt megcélzó kezelésekkel kezd változni.
- Vastagbélrák esetén annak meghatározása, hogy a tumor valószínűleg örökletes (pl. Lynch-szindróma) vagy szórványos (nem örökletes).
- Egyes rákos megbetegedéseknél, például a pajzsmirigyráknál, hogy segítsen meghatározni a pontos diagnózist.
- Egyéb felhasználások: A BRAF teszt (folyékony biopszián keresztül) a közeljövőben felhasználható a melanoma kezelés nyomon követésére, a műtét után az emberekben fennmaradó rákos sejtek kimutatására (minimálisan maradvány betegség) vagy a korai relapszus tesztelésére.
Rákok, amelyeknél a BRAF teszt elvégezhető
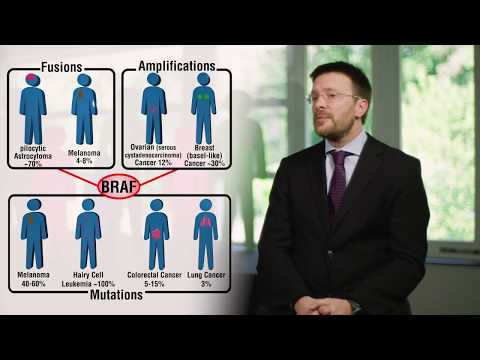
A BRAF-mutációk számos különböző ráktípusban megtalálhatók, bár ezeknek a mutációknak a gyakorisága jelentősen eltér. Nagyon gyakoriak metasztatikus melanoma és néhány más daganat esetén. Míg ritkábban fordul elő olyan daganatokban, mint a nem kissejtes tüdőrák, ezeknek a mutációknak a megtalálása fontos, mivel rendelkezésre állnak olyan kezelési lehetőségek, amelyek meghosszabbíthatják az életet. Orvosa javasolhatja a BRAF tesztet, ha rendelkezik:
- Melanoma (metasztatikus / 4. vagy 3. stádium)
- Nem kissejtes tüdőrák
- Colorectalis rák
- Pajzsmirigyrák (anaplasztikus pajzsmirigyrák és papilláris pajzsmirigyrák)
- Súlyos petefészekrák (az epitheliális petefészekrák egy típusa)
- Egyéb daganatok, mint például a non-Hodgkin-limfóma, egyes agydaganatok (például gyermekeknél a ganglioglioma és a pilocytás astrocytoma), a nyelőcsőrák és még sok más
Ha a tesztelés kész
Ideális esetben a BRAF-tesztet akkor végezzük, amikor először diagnosztizálunk egy daganatot (áttétes vagy 3. stádiumú melanoma). Ezt gyakran akkor is elvégzik, ha a tumor előrehalad vagy áttétet ad, amikor a BRAF státusza megváltozhat. A diszkordancia kifejezést arra használják, hogy leírják, hogyan lehet egy tumor kezdetben BRAF negatív, de előrehaladtával BRAF pozitívvá válhat. Ezt könnyebb megérteni, ha rájövünk, hogy a rákos megbetegedések folyamatosan változnak, és növekedésük során új mutációk alakulnak ki.
A BRAF státus megváltozhat, és egy olyan daganat, amely kezdetben negatív diagnózis esetén, pozitív lehet, ha előrehalad vagy megismétlődik.
Típusok
A BRAF mutációknak többféle típusa létezik, a BRAF V600E és a BRAF V600K a leggyakoribb. A nem BRAF V600 mutációk gyakoribbak a melanomán kívüli egyéb daganatokban, bár ezen egyéb mutációk jelentősége sok esetben még mindig nem ismert. E különböző típusok jelenléte fontos a tesztelés során, mivel egyes vizsgálati módszerek csak a BRAF V600E mutációkat képesek kimutatni, míg mások szélesebb tartományt.
BRAF tesztelés rák nélküli embereknél
Amint megjegyeztük, a rákos betegek BRAF-mutációi szinte mindig megszerzett BRAF-mutációk, de előfordulhatnak örökletes BRAF-mutációk is. Ezenkívül a BRAF-mutációk más nem rákos betegségekkel is társulhatnak. Más szavakkal, ha azt mondják, hogy BRAF-mutációja van, ha még nem diagnosztizálták nálunk a rákot, az nem azt jelenti, hogy rákja van (bár ez megnövekedett kockázattal járhat).
Vizsgálati módszerek
Számos különféle vizsgálati módszer áll rendelkezésre a BRAF jelenlétének felkutatására, és ezeknek a módszereknek a részletes ismertetése meghaladja a cikk kereteit. Két különböző típusú vizsgálat létezik, amelyeket fontos megvitatni, mivel a BRAF-mutáció megtalálásának valószínűsége, ha van ilyen, ezen módszerek között változhat.
- Gyors tesztelés: Egyes gyors tesztelési módszerek csak a V600E mutációkat képesek kimutatni, amelyek a melanóma során leggyakrabban előforduló BRAF mutációk
- Átfogó genomi profilálás (DNS-szekvenálás): A DNS-szekvenálás képes kimutatni más típusú BRAF mutációkat, valamint más gének mutációit vagy genomiális változásait, amelyek befolyásolhatják a tumor viselkedését
Mindkét módszernek vannak előnyei és hátrányai, például a hisztokémiai eredmények sokkal hamarabb elérhetők lehetnek, míg az átfogó genomi profilozás nagyobb érzékenységgel bír a BRAF mutációk kimutatásában.
Tüdőrák
A tüdőrák esetében általában a következő generációs szekvenálást végzik, és a metasztatikus, nem kissejtes tüdőrák esetében költséghatékony és legátfogóbbnak bizonyult. A tüdőrák esetén számos más potenciálisan kezelhető szintén kimutatható mutációk, amelyek tovább indokolják az átfogó tesztelést. Ezenkívül a BRAF mutációk rezisztencia mutációkként alakulhatnak ki, olyan mutációkként, amelyek egy célzott terápia más formájával (például EGFR-gátlókkal) kezelt daganatban fordulnak elő, hogy elkerüljék a gyógyszeres kezelést.
Melanóma
A melanoma esetében a DNS-szekvenálás az arany standard, bár gyakran végeznek gyors teszteket. Van azonban néhány bizonyíték arra, hogy az átfogó genomi profilalkotás előnyökkel járhat (vagy legalábbis figyelembe kell venni azokat az embereket, akiknek más módszerekkel negatív a BRAF-tesztje).
Egy 2019-es alapján PLoS One tanulmány szerint az immunkémia hatékony a V600E mutációk kimutatásakor, de azoknak az embereknek, akiknek negatív tesztje van, molekuláris tesztet kell végezni más BRAF mutációk keresése érdekében.
Egy másik 2019-es tanulmány azt találta, hogy az átfogó génprofilozás (hibrid elfogáson alapuló következő generációs szekvenálás) képes volt kimutatni az aktiváló BRAF-változásokat a korábban negatívan tesztelt tumorok jelentős részében. Ennek a tanulmánynak a következtetése az volt, hogy mivel a BRAF-mutációk jelenlétének kimutatása olyan kezelésekhez vezethet, amelyek bizonyítottan előnyökkel járnak, átfogó génprofilozásra kell gondolni, különösen azoknál az embereknél, akik eredetileg negatívnak bizonyultak.
A gyorstesztek összehasonlítása érdekében egy 2018-as tanulmány az immunhisztokémiát, a Droplet Digital PCR tesztet és az Idylla Mutation Platformot vizsgálta. Az egyik vizsgálatban az Idylla mutációs tesztet gondolták a legalkalmasabbnak, mivel ez volt a leggyorsabb, és más gyors tesztekkel ellentétben a BRAF V600E-n kívül más mutációkat is képes azonosítani.
A BRAF-fel együtt megrendelt tesztek
Nincsenek olyan tesztek, amelyek helyettesíthetik a BRAF-tesztet, mivel a BRAF-pozitív és a negatív daganatok ugyanazok a mikroszkóp alatt.Más azonosított mutációk azonban hasznosak lehetnek, mivel egyes mutációk jelenléte általában arra utal, hogy BRAF-mutáció nem lesz jelen. A teszt olyan információkat is nyújthat, például a PD-L1 szinteket, amelyek hasznosak lehetnek a legjobb kezelési lehetőségek kiválasztásában.
Mintavételi módszerek
A BRAF-vizsgálat elvégezhető egy tumorszöveti mintán, vérvizsgálattal (folyékony biopszia), vagy mindkettővel, bár a tumorszövet továbbra is az "aranystandard".
Tumortesztelés vagy "Biopsziamentes" tesztelés
A BRAF-tesztet leggyakrabban egy szövetmintán végzik, amelyet biopszia vagy tumor eltávolítása során vettek. Ez azonban kihívásokat jelenthet, mivel a szövet előállításához szükséges biopsziás eljárások invazívak, és még akkor is előfordulnak olyan esetek, amikor nincs elegendő szövet a teszt elvégzéséhez. Mivel annak tudatában, hogy van-e BRAF-mutáció, fontos következményei lehetnek a kezelésben azon túl, hogy megtudjuk, reagál-e egy személy egy BRAF-gátlóra (a BRAF-negatív, de BRAF-gátlókkal kezelt daganatok valójában gyorsabban haladhatnak, mintha nem kezelték volna őket) , a kutatók más módszereket kerestek hasonló eredmények elérésére.
Agydaganatok esetén a vizsgálat elvégezhető a gerincvelő segítségével nyert cerebrospinalis folyadék mintáján is.
Folyékony biopszia
A daganatok, különösen az előrehaladottabb daganatok, folyamatosan a tumor darabjait engedik a véráramba. Míg az egész rákos sejtek megtalálása kihívást jelent, a kutatók most már képesek kimutatni a sok tumor keringő tumor DNS-ét. Ha megtalálják, ezt a DNS-t mutációk és más genomiális változások szempontjából is tesztelhetjük.
A folyékony biopszia hátránya, hogy a technika viszonylag új, és nem minden daganat, különösen a korai stádiumú daganatok eredményeznek keringő DNS-t, amely kimutatható.
Ennek a módszernek egyértelmű előnye, hogy csak egyszerű vérvizsgálatot igényel, és mivel a vérvizsgálat általában gyorsan elvégezhető, hamarabb elérhetők lehetnek eredmények. Emiatt úgy gondolják, hogy a folyékony biopsziákat időben fel lehet használni a rák szorosabb figyelemmel kísérésére. (Jelenleg általában megtudjuk, hogy egy daganat rezisztenssé vált egy olyan gyógyszerrel szemben, mint a BRAF-gátló, mert látható, hogy egy olyan tanulmányban, mint például a számítógépes tomográfia [CT], ismét növekszik. Egy folyékony biopszia potenciálisan kimutathatja ez az ellenállás még azelőtt, hogy a rák láthatóan növekedne, így azonnal más kezelést lehetne kezdeni).
A folyékony biopszia másik előnye, hogy lehetővé teszi a mutáció kimutatását a tumor bármely pontján. A rákok folyamatosan új mutációkat fejlesztenek ki, és a tumor egyik részében jelen lévő mutációk nem lehetnek jelen a másikban (tumor heterogenitás). Egy ideje ismert, hogy mutáció lehet jelen, amikor a daganat előrehalad, vagy csak a metasztázis helyén található meg. Ez bekövetkezhet belül daganat is. A tumor biopszia ezzel ellentétben csak arra utal, ha mutáció van jelen a tumor azon részében, amelyből biopszia során vettek mintát.
Folyékony biopsziák a rák kezelésébenTüdőrák
A tüdőrák esetében egy 2018-as tanulmány valójában azt találta, hogy a folyékony biopsziás minták ugyanolyan jóak, mint a szövetvizsgálatok a kezelhető mutációk kimutatásában. Bizonyos esetekben genomiális változást lehetett tapasztalni csak daganatmintán vagy csak folyékony biopszián, de általában jó volt az összefüggés. Néhány onkológus most azt javasolja, hogy mindkét tumorszövet és vér, ha potenciálisan kezelhető mutációkat és egyéb genomiális változásokat keresnek.
Melanóma
A melanoma esetében a folyékony biopszia alkalmazása kevésbé volt hasznos ("alacsonyabbrendűnek" tekinthető), mint a BRAF-mutációk szövetvizsgálata, de ez is változhat. Néhány onkológus most szöveti vizsgálatot (amikor minta nyerhető) és folyékony biopsziát (Guardant 360) is elrendel.
A folyékony biopszia alátámasztására egy 2018-as tanulmány mutációt talált két melanómában szenvedő embernél, amelyeket a daganatvizsgálat során nem észleltek, és mindkét beteg válaszolt a célzott terápiára.
Korlátozások
A BRAF-tesztelés általános korlátja az, hogy a szövet nem elegendő a biopsziás mintán történő vizsgálat elvégzéséhez. Remélhetőleg a folyékony biopsziák a közeljövőben javíthatják ezt a korlátozást.
A bármilyen laboratóriumi vizsgálattal a BRAF teszt laboratóriumi hibának minősül.
Kockázatok és ellenjavallatok
A BRAF-teszt elsődleges kockázata a minta megszerzésére alkalmazott eljárás. Ez a rák típusától, a rák helyétől, a személy általános egészségi állapotától és egyebektől függően változhat. Folyékony biopsziával (keringő tumor DNS) a kockázat hasonló a többi vérvételhez, kis számú embernél véraláfutás vagy vérkép alakul ki a vérvétel helyén.
Hamis pozitívumok és negatívumok
Egy másik lehetséges kockázat, hogy a teszt lehet hamis pozitív vagy hamis negatív. Hamis negatív teszttel olyan személyek, akik egyébként reagálhatnak az anti-BRAF terápiákra, nem ajánlják fel ezeket a kezeléseket.
A hamis pozitív eredményeknél vannak kockázatok is. Ha a BRAF negatív tumorokat (a továbbiakban: „BRAF vad típus”) BRAF inhibitorokkal kezelik, az valóban serkentheti a daganatok növekedését (a gyógyszerek aktiválhatják a daganat növekedési útvonalát), ami a rák. Ez azt is eredményezheti, hogy egy személy nem kap hatékony terápiát.
A teszt előtt
Mielőtt orvosa elrendeli a BRAF-tesztet, meg akarják tudni, hogy milyen típusú rákja van, hol keletkezett, és milyen kórtörténettel rendelkezik. A BRAF mutációk nagyobb valószínűséggel találhatók meg egyes daganatoknál, mint mások (például nagyon gyakori a "nyálkahártya" melanomákban, például a végbél melanómájában, és ritkábban néhány más daganattal). Kezelőorvosa meg akar tudni minden olyan kezelést, amelyet eddig kapott (például tüdőrák esetén BRAF-mutáció alakulhat ki, miután egy személyt más típusú, a rák kezelésére szolgáló gyógyszerrel kezeltek).
Orvosa arról is beszél, hogy a vizsgálatot szövetmintán, vérmintán (folyékony biopszia) vagy mindkettőn kell-e elvégezni. Ha szövetmintára van szükség, és nincs elegendő szövet a korábbi biopsziákból, szükség lehet ismételt biopsziás eljárásra. Ha igen, megvitatja a biopsziás eljárás kockázatait és előnyeit.
Időzítés
A vizsgálathoz szükséges idő jelentősen változhat attól függően, hogy szövet- vagy vérmintára van-e szükség, és a vizsgálat típusától. Szövetmintával, ha újabb biopsziára van szüksége, hozzá kell adnia az időt az ütemezéshez és a biopsziához a BRAF-teszt elvégzéséhez szükséges időhöz. A gyors tesztek csak néhány nap múlva adhatnak eredményt. A folyamat következtében a következő generációs szekvenálás akár két-négy hétig is eltarthat, mire az eredmények rendelkezésre állnak.
Elhelyezkedés
A vizsgálat helye attól függ, hogy orvosa már rendelkezik-e daganatos szövetekkel (egy korábbi biopsziából vagy műtétből származik), vagy szükség lesz-e ismételt biopsziára vagy vérvételre. Vérvétel klinikai körülmények között végezhető, míg a biopszia műtéti beállítást igényelhet.
Étel és ital
Ha biopsziát végez, az eljárás előtt korlátozások lehetnek. A BRAF-tesztet megelőzően általában nincsenek külön diéták vagy élelmiszer-korlátozások.
Költség- és egészségbiztosítás
A BRAF mutációk vizsgálata meglehetősen költséges lehet, ezért fontos, hogy a teszt előtt beszéljen orvosával az esetleges zseben kívüli költségekről.
Egyes biztosítótársaságok könnyen fedezik a daganatvizsgálatot és a folyékony biopsziát, míg mások csak egyet. Még a fedezet megléte esetén is előfordulhat, hogy előzetes engedélyre van szükség, és zsebköltségei lehetnek.
A költségek nagymértékben változhatnak a tesztelés típusától, valamint a rák típusától függően. A gyors tesztek ("hot spot" tesztek, amelyek csak egyetlen vagy néhány specifikus mutációt keresnek) sokkal olcsóbbak, mint a teljes exon szekvenálás.
Ha a BRAF-teszt költsége nehézkes, vannak lehetőségek a segítségnyújtásra. Ha 3. vagy 4. stádiumú melanómája van, a Novartis (a Quest Diagnostics-szel együtt) felajánlja a Tudjon most tesztelési programot. Ez a program ingyenes biopszia-tesztet (folyékony biopszia-tesztet) biztosít melanomában szenvedők számára ingyenesen.
Mit hozni
Mint minden látogatáskor, fontos, hogy hozza magával a biztosítási kártyáját. Vigyen magával minden laboratóriumi vagy patológiai vizsgálatot, amelyet egy külső klinikán vagy kórházban végeztek, hacsak nem biztos abban, hogy orvosa hozzáfér ezekhez.
A teszt során
Amikor orvosa vizsgálathoz benyújtja vérét vagy daganatos szövetét, ki kell töltenie egy űrlapot, amely számos részletet ismertet a rákkal kapcsolatban. Kérdezhet, hogy ez a lehető legpontosabb legyen. Felkérhetik űrlap kitöltésére is, amelyben kijelenti, hogy Ön felel a költségek bármely olyan részéért, amelyet nem fedez a biztosítás.
A teszt után
Amikor a teszted befejeződik (akár vérvizsgálat, akár biopszia), akkor hazatérhetsz, amikor jól teljesítesz. Ha vérvétel történt, akkor a helyszínen néhány zúzódást észlelhet. Biopszia esetén az előforduló tünetek mind a biopszia típusától, mind a helyétől függenek, ahol azt elvégzik.
Orvosa tájékoztatja Önt, ha időpontot kell rendelnie, hogy megismerje eredményeit, vagy ha Önt hívják, amikor rendelkezésre állnak.
Várakozás az eredményekre
A BRAF tesztelés (és általában a genomiális változások tesztelése) egyik legnagyobb kihívást jelentő aspektusa vár. Egyes rákos megbetegedések esetén a BRAF-gyorstesztek elvégezhetők, és az eredményeket egy héten belül megkapja. A BRAF gyorstesztjeivel ellentétben azonban a DNS-szekvenálási tesztek (következő generációs szekvenálás) időnként két-négy hétig is eltarthatnak, mire az eredmények rendelkezésre állnak. Ez az idő nem tranzitidő (pl. Az az idő, amely egy próbadarabnak a laboratóriumba utazásához szükséges, vagy az az idő, amely egy orvosnak meg kell néznie és felül kell vizsgálnia az eredményeket), hanem az a tényleges idő, amely a teszt futtatásához szükséges.
A tüdőrák esetén ez nagyon szoronghatja az orvosokat és a betegeket egy másik kezelés megkezdéséről. Mégis, bizonyos esetekben egy másik kezelés (például kemoterápia) elkezdése több kárt okozhat, mint hasznot. Természetesen ez óriási mértékben változik, és csak Ön és onkológusa mérlegelheti az adott rákkal való várakozás előnyeit és kockázatait.
Az eredmények értelmezése
A BRAF teszt eredményeinek értelmezése az alkalmazott módszertől, a rák típusától és a jelen lévő BRAF mutáció típusától függ.
Eredmények
Az eredmények bemutatása az elvégzett teszttől függ. Gyors teszteléssel olyan eredményt kaphat, amely szerint a mutáció jelen van vagy hiányzik.
DNS-profilozással számos különböző mutációról lehet beszámolni a laboratóriumi eredményekről. Ezek némelyikének jelenléte segíthet az onkológus további jellemzésében a daganatban, de még mindig sok minden ismeretlen. Számos kimutatható mutáció (a BRAF kivételével) jelentősége egyelőre ismeretlen.
Ha BRAF-mutációt találnak Önnél, orvosa beszélni fog a kezelés lehetőségeiről, beleértve azt is, hogy mire számíthat a hatékonyság tekintetében a többi rendelkezésre álló kezelési lehetőséghez képest.
Utánkövetés
A BRAF-tesztet követő nyomon követés a teszt eredményeitől és a rákos megbetegedésektől függ.
Ha a tesztelés negatív
Ha a BRAF teszt negatív a szövetvizsgálaton (a rák típusától függően), akkor folyékony biopsziát lehet fontolóra venni (vagy fordítva). Hasonlóképpen, ha a BRAF teszt negatív egy gyors teszten, akkor fontolóra lehet venni az átfogó génprofilozást.
A tumor progressziója és / vagy terjedése
Azok számára, akiknél a daganat progressziója alakul ki, vagy ha ez más régiókra is átterjed, fontolóra vehető az ismételt teszt. A daganatok folyamatosan változnak, és az adott mutációk vagy egyéb genomiális változások hajtás a daganat növekedése is megváltozhat. Az ismételt vizsgálat fontos a melanóma esetében, mivel egy olyan daganat, amely eredetileg nem volt BRAF pozitív, növekedésével BRAF pozitívvá válhat.
A mutáció státuszának változása jól ismert a nem kissejtes tüdőrák esetében, és a BRAF mutációk gyakran "rezisztencia mutációként" fejlődnek ki olyan tumorokban, amelyek EGFR pozitívak (de BRAF negatívak) és EGFR inhibitorokkal kezeltek.
Egyéb szempontok
A BRAF teszteléssel számos más szempont is jár. A melanomával kapcsolatban jelenleg arról van szó, hogy melyik kezelési lehetőség a legjobb azoknak az embereknek, akiknek BRAF-mutációja van. A célzott terápia (BRAF-gátlók) általában sok ember számára működik, de az ellenállás gyakran egy éven belül kialakul.
Ezzel szemben az immunterápia kevesebb ember számára hatékony, de ha hatékony, hosszabb reakcióidőt eredményezhet. Ezt a kérdést mindenkinek meg kell vitatnia onkológusával, akinek BRAF-pozitív melanomája van. A legújabb kutatások azonban e terápiák (triplett terápia) és ígéretes korai eredmények kombinációját vizsgálják.
Hármas terápia a BRAF pozitív melanoma eseténBizonyos esetekben a második vélemény megszerzése nagyon hasznos. Sok orvos azt javasolja, hogy kapjon második véleményt az egyik nagyobb Országos Rákintézet által kijelölt rákközpontban, ahol nagyobb valószínűséggel vannak olyan onkológusok, akik a rák specifikus típusára (és talán molekuláris altípusára) szakosodtak.
Egy szó Verywellből
A BRAF tesztelése és az eredményekre való várakozás nagy szorongáshoz vezethet. Miután az embernél rákot diagnosztizáltak, nagyon nehéz ülni és várni, ahogy azt elképzelheti, hogy a daganata növekszik. Amikor végre elérted az eredményeidet, a szorongás másik forrása lehet. Mit csinálsz most? A rákkezelés számos előrelépése szerencsére sok új lehetőséget hozott, ugyanakkor szívbemarkoló lehet az, hogy melyik opciót választja Önnek.
Hogyan lehet a saját szószólója rákos betegkéntA támogatási rendszer elérése és a rá támaszkodás elengedhetetlen. Ez nem az az idő, hogy erős legyünk, hanem az az idő, amikor szeretetet és bátorítást kapunk. A hasonló utazás előtt álló más rákos túlélőkkel való kapcsolat szintén felbecsülhetetlen. Ez nem csak több támogatást hozhat, de a betegségben szenvedő betegtársak néha olyan szavakkal is megmagyarázhatják a dolgokat, amelyek nem hasonlítanak idegen nyelvre.