Tartalom
Az ALK-pozitív tüdőrák egy nem kissejtes tüdőrák (NSCLC), amely az anaplasztikus limfóma kináz (ALK) nevű gén mutációját hordozza magában. Pontosabban, ez egy gén átrendeződés - az ALK és egy másik gén, az echinoderm mikrotubulushoz társuló fehérjeszerű 4 (EML4) fúziója. Ez a kóros fúzió arra készteti a sejtenzimeket (fehérjéket), hogy jeleket küldjenek a mutált rákos sejteknek, mondván, hogy osztódjanak szét. és a szokásosnál gyorsabban szaporodik, ami tovább terjeszti a betegséget.A genetikai mutációkhoz kapcsolódó más tüdőrák típusokhoz hasonlóan az ALK átrendeződését most is meglehetősen hatékonyan lehet célzott terápiás gyógyszerekkel kezelni, lehetővé téve a rák kezelését. Ez jobb túlélési arányhoz vezetett a betegek körében a tüdőrák minden szakaszában.
Okoz
Az ALK átrendeződés az NSCLC-s betegek 3–5% -ánál fordul elő. Ez első ránézésre kevésnek tűnhet, de figyelembe véve az évente tüdőrákkal diagnosztizált emberek számát, ez azt jelenti, hogy körülbelül 10 000 újonnan minden évben diagnosztizált ALK-incidenseket az Egyesült Államokban.
A tüdőrákban jelenlévő mutációk típusai a tüdőrák típusától függően változnak. Az ALK-mutáció messze a leggyakrabban a nem kissejtes tüdőrákban szenvedő embereknél, az úgynevezett tüdő-adenokarcinómában szenvedő embereknél fordul elő. Ritka esetekben azonban ALK-tüdőrákot találtak a tüdőben lévő laphámsejtes betegeknél ( a nem kissejtes tüdőrák egy másik típusa) és a kissejtes tüdőrák.
Ez a fúziós gén nem örökletes mutáció, mint a BRCA mutációk egyes emlő- és más rákos embereknél. Azok az emberek, akiknek az EML4-ALK fúziós génje szempontjából pozitív a tüdőrák, nem olyan sejtekkel születtek, amelyeknél ez a mutáció volt, és nem örökölték ezt a mutációt a szüleiktől.
Ehelyett ez egy megszerzett mutáció, amely számos tényező miatt egyes sejtekben kialakul. Például a környezeti rákkeltőknek való kitettség károsíthatja a géneket és a kromoszómákat, és mutált sejteket eredményezhet.
Ezenkívül az EML4-ALK fúziós gén nem kizárólag a tüdőrákhoz kapcsolódik. Megtalálható neuroblastomában és anaplasztikus nagysejtes limfómában szenvedőknél is.
Kockázati tényezők
Bizonyos embereknél nagyobb az esély az ALK fúziós génre:
- Fiatalabb betegek (55 éves és fiatalabbak)
- Olyan emberek, akik soha nem dohányoztak (vagy nagyon keveset dohányoztak)
- Nők
- A kelet-ázsiai nemzetiségűek
Vizsgálatok során a 40 évesnél fiatalabb NSCLC betegek az esetek 34% -ában pozitívnak találták az EML4-ALK fúziós gént, szemben az NSCLC-ben szenvedő minden életkorú emberek körülbelül 5% -ával.
Az öröklött és megszerzett tüdőrák megértéseDiagnózis
Az ALK átrendeződését genetikai teszteléssel (más néven molekuláris profilozással) diagnosztizálják. Az orvosok szöveti biopsziával szereznek tüdődaganat mintát, és megvizsgálhatják a folyékony biopsziával nyert vérmintát. Ezeket a mintákat olyan biomarkerek után ellenőrizzük, amelyek azt mutatják, hogy az ALK mutáció jelen van.
A kutatók azt is megvizsgálják, hogyan lehet megállapítani, hogy van-e ALK-mutáció előtt genetikai tesztet végeznek, vagy ha helyettesítik a molekuláris profilozást.
Néhány dolog, ami arra utal, hogy ALK mutáció jelen lehet:
- Vérmunka: A carcinoembryonic antigen (CEA) nevű teszt általában negatív vagy alacsony szintet mutat az ALK mutációval rendelkező embereknél.
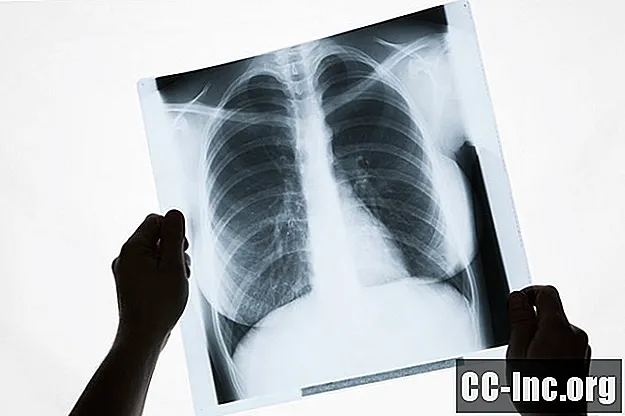
- Radiológia: Az ALK-pozitív tüdőrák képalkotása másnak tűnik, mint más típusú NSCLC-k esetében, ami segíthet az orvosoknak a mutáció korai felismerésében.
Kit kell tesztelni ALK mutáció miatt?
Számos szervezet működött együtt az erre vonatkozó iránymutatások kidolgozásában.Az egyetértés az, hogy minden előrehaladott stádiumú adenokarcinómában szenvedő beteget meg kell vizsgálni az ALK és más kezelhető genetikai mutációk szempontjából, nemtől, fajtól, dohányzástörténettől és egyéb kockázati tényezőktől függetlenül.
Ezek az irányelvek kissé rugalmasak. Az orvosok javasolhatják, hogy más emberek is végezzenek tesztelést, és egyesek ragaszkodnak ehhez mindenki az NSCLC-vel diagnosztizált genetikai teszteket végeznek.
Kezelés
Az ALK átrendeződését orális gyógyszerekkel kezelik, amelyek az előrehaladott tüdőrák daganatok csökkentésére szolgálnak.
Azokat a gyógyszereket, amelyeket az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) jóváhagyott az ALK-pozitív tüdőrák kezelésére, ALK-gátlóknak nevezzük, és a következők:
- Alecensa (alektinib)
- Alunbrig (brigatinib)
- Lorbrena (lorlatinib)
- Xalkori (crizotinib)
- Zykadia (ceritinib)
Ha az ALK gén átrendeződésének eredménye pozitív, az első kúra kemoterápia helyett általában ALK inhibitorokat alkalmaz. Bár az orvosok néha elkezdhetik a kemoterápiát, és csak akkor kezdhetik el az ALK gyógyszereket, ha a terápia leállt.
Hogyan működnek az ALK-gátlók
A tirozin-kinázok a sejtek olyan elemei, amelyek lehetővé teszik a jelek egyik sejtből a másikba történő továbbítását, és a tirozin-kináz minden sejtje receptor fogadja ezeket a jeleket.
Az ALK-célzott terápiás gyógyszerek működésének megértéséhez gondoljon a sejt tirozin-kináz-receptorára, mint zárra, és a tirozin-kináz-fehérjére (amely az üzenetet tartalmazza), mint kulcsra. Ha ALK mutációja van, akkor rendellenes kulcsa van. Amikor a mutált kulcsot „behelyezik”, a sejt növekedési központjába jeleket küldenek, amelyek a rákos sejteket megállás nélkül osztják fel.
Az olyan gyógyszerek, mint a Xalkori (crizotinib), a kulcslyuk blokkolásával hatnak, mintha betonnal töltenék be. Ennek eredményeként a jel, amely a rákos sejteket osztja és növekszik, soha nem kerül kommunikációra.
A daganatok évekig kezelhetők ezekkel a gyógyszerekkel, biztosítva, hogy a sejtek ne terjedjenek.
Cél: Irányítás, nem gyógyítás
Fontos szem előtt tartani, hogy a tirozin-kináz gátlók nem gyógyírok a tüdőrákra, sokkal inkább olyan dolgok, amelyek lehetővé teszik a daganat kordában tartását (akárcsak a cukorbetegség kezelésére szolgáló gyógyszer, a betegség kontrollálható, de nem gyógyítja meg). Remélhetőleg a jövőben a tüdőrákot más krónikus betegségekhez hasonlóan kezelhetik.
Ellenállás
A tüdőrák kezdetben nagyon jól reagálhat a célzott terápiás gyógyszerekre. A betegek azonban idővel szinte mindig rezisztenssé válnak.
A rezisztencia a kezelés kezdetétől számított kilenc héten belül kialakulhat, de néhány ember számára a gyógyszerek sok éven át továbbra is hatékonyak lehetnek.
Ha ellenállása alakul ki az ALK-gátlóval szemben, orvosa új gyógyszert vagy gyógyszerek kombinációját fogja kipróbálni. Az új gyógyszereket továbbra is klinikai vizsgálatokban tanulmányozzák olyan emberek számára, akiknél rezisztencia alakul ki.
Szükség lehet a gyógyszerek beállítására is, mert a rák idővel tovább mutálódhat. Néha egy másik kezelhető mutációt (például EGFR) célzó gyógyszer működhet, annak ellenére, hogy a daganat eredetileg nem volt pozitív az EGFR mutáció szempontjából. Például a Lorbrena (loratinib) gyógyszert azoknak az embereknek engedélyezték, akiket korábban más ALK-gátlókkal kezeltek, és hatásosnak bizonyult azoknak az embereknek a felénél, akik rezisztenssé váltak ebben az osztályban más gyógyszerekkel szemben. A hatás medián időtartama 12,5 hónapok
Az E-vitamin összetevői jelentősen befolyásolhatják egyes ALK-gátlókat. Beszéljen orvosával, mielőtt rákkezelés alatt szedne E-vitamint vagy bármilyen kiegészítőt.
Kezelés mellékhatásai
Mint más rákos gyógyszerek, az ALK-gátlóknak is vannak mellékhatásai. Ezeknek enyhéknek kell lenniük a kemoterápia mellékhatásaihoz képest, de mégis kényelmetlenek és megzavarhatják a mindennapi életet.
A Xalkori (crizotinib) gyakori mellékhatásai a következők:
- Látászavarok
- Hányinger
- Hasmenés
- Hányás
- Ödéma
- Székrekedés
- Megnövekedett transzaminázszint (májkárosodás miatt)
- Fáradtság
- Csökkent étvágy
- Felső légúti fertőzés
- Szédülés
- Neuropathia
Egy másik ritka, de súlyos mellékhatás, amelyet észleltek, az interstitialis tüdőbetegség kialakulása, amely végzetes lehet.
Költség
A rákos sejtek rendellenességeit célzó újabb gyógyszerek, például az ALK mutációk, gyakran meredek árcédulával járnak. De vannak lehetőségek.
Azok számára, akiknek nincs biztosításuk, vannak állami és magánprogramok, amelyek segíthetnek. A biztosítással rendelkezők számára a copay segítő programok segíthetnek a költségek fedezésében.
Bizonyos esetekben a gyógyszer gyártója csökkentett költséggel tud gyógyszereket szállítani. És ami fontos, lehet, hogy ingyenes kezelést kaphat, ha részt vesz egy klinikai vizsgálatban.
Prognózis
Míg az NSCLC általános ötéves túlélési aránya körülbelül 25%, amely 2–7% -ra csökken az előrehaladott stádiumú tüdőrák esetében, a kutatók azt találták, hogy a 4. stádiumú ALK-pozitív tüdőrákos betegek túlélési mediánja 6,8 év Ez a túlélési arány igaz azokra is, akiknek tüdőrákja átterjedt az agyban (agyi áttétek).
Ben megjelent tanulmány ANew England Journal of Medicine megállapította, hogy a Xalkori-val (crizotinib) végzett kezelés kb. 10 hónapos átlagos progressziómentes túlélést eredményez.Nagyon 50-60% -os válaszarány van a gyógyszerre. Ez drámai megállapítás, mert a tesztben részt vevő személyek már nem tudták kimutatni a kemoterápia előrehaladását, és várható válaszarányuk 10% volt, az előrejelzett átlagos progressziómentes túlélés körülbelül három hónap volt.
Bár a tanulmányok nem mutatják az összes túlélés növekedését az ALK-átrendeződési kezelések mindegyikénél, egyértelmű javulás tapasztalható ezeknél a gyógyszereknél kínált életminőségben, és lehetőség van progresszió nélküli életre súlyos mellékhatások nélkül.
Mit jelent valójában a túlélési arány a rákkalEgy szó a Wellwell-től
A kulcsa annak, hogy az ALK-mutációkra vonatkozó gyógyszereket kihasználhassuk, genetikai tesztelés. Míg sok orvos azt javasolja, hogy mindenkit értékeljenek NSCLC-vel, sok betegnél nem végeznek molekuláris profilozást.
Beszélje meg a tesztelés lehetőségét orvosával. Ha lehetséges, fontolja meg egy második vélemény megszerzését egy rákközpontban, amely nagy mennyiségű tüdőrákos beteget lát, és jobban támogathatja a vizsgálandó döntést.
- Ossza meg
- Flip
- Szöveg